文献解析

近日,上海交通大学医学院附属仁济医院彭雅雯博士、何征宇教授团队在《Experimental & Molecular Medicine》期刊发表重要研究成果:“PGC-1α介导肺成纤维细胞释放迁移体促进巨噬细胞MMT参与SAPF发生”(DOI: 10.1038/s12276-025-01426-z)。
该研究首次揭示:在LPS诱导的SAPF模型中,肺成纤维细胞通过迁移体(Migrasomes)释放线粒体DNA(mtDNA),诱导巨噬细胞向肌成纤维细胞转化,从而加速肺纤维化进展。而PGC-1α作为线粒体稳态调节因子,其表达下调是促发该链式反应的关键因子。
背景简介
脓毒症相关性肺纤维化(Sepsis-associated pulmonary fibrosis, SAPF)是脓毒症引发的急性呼吸窘迫综合征(ARDS)进展过程中的一个关键病理阶段,其发生机制尚不清晰。尽管肺成纤维细胞的聚集和活化在肺纤维化的发生中起核心作用,近年来,“巨噬细胞-肌成纤维细胞转化(Macrophage–myofibroblast transition, MMT)”被提出为肌成纤维细胞来源的新模式,而该过程的启动信号及其调控机制亟待揭示。
项目研究
在LPS诱导的SAPF模型中,研究者观察到明显的巨噬细胞向肌成纤维细胞转化(MMT)现象,包括M1型和M2型巨噬细胞均可转化为表达α-SMA的MMT细胞,参与纤维化灶的形成。
单细胞转录组和RNA速度分析进一步明确了这一细胞命运转换的轨迹。同时,LPS刺激显著增强了成纤维细胞的迁移能力,并诱导其释放大量迁移体(migrasomes)。
进一步研究表明,这些迁移体可携带mtDNA并被巨噬细胞摄取,从而诱导其表达α-SMA并启动MMT过程。阻断迁移体传递或抑制其形成均可显著抑制MMT,提示迁移体在成纤维细胞-巨噬细胞间信号传递及纤维化进展中发挥关键作用。
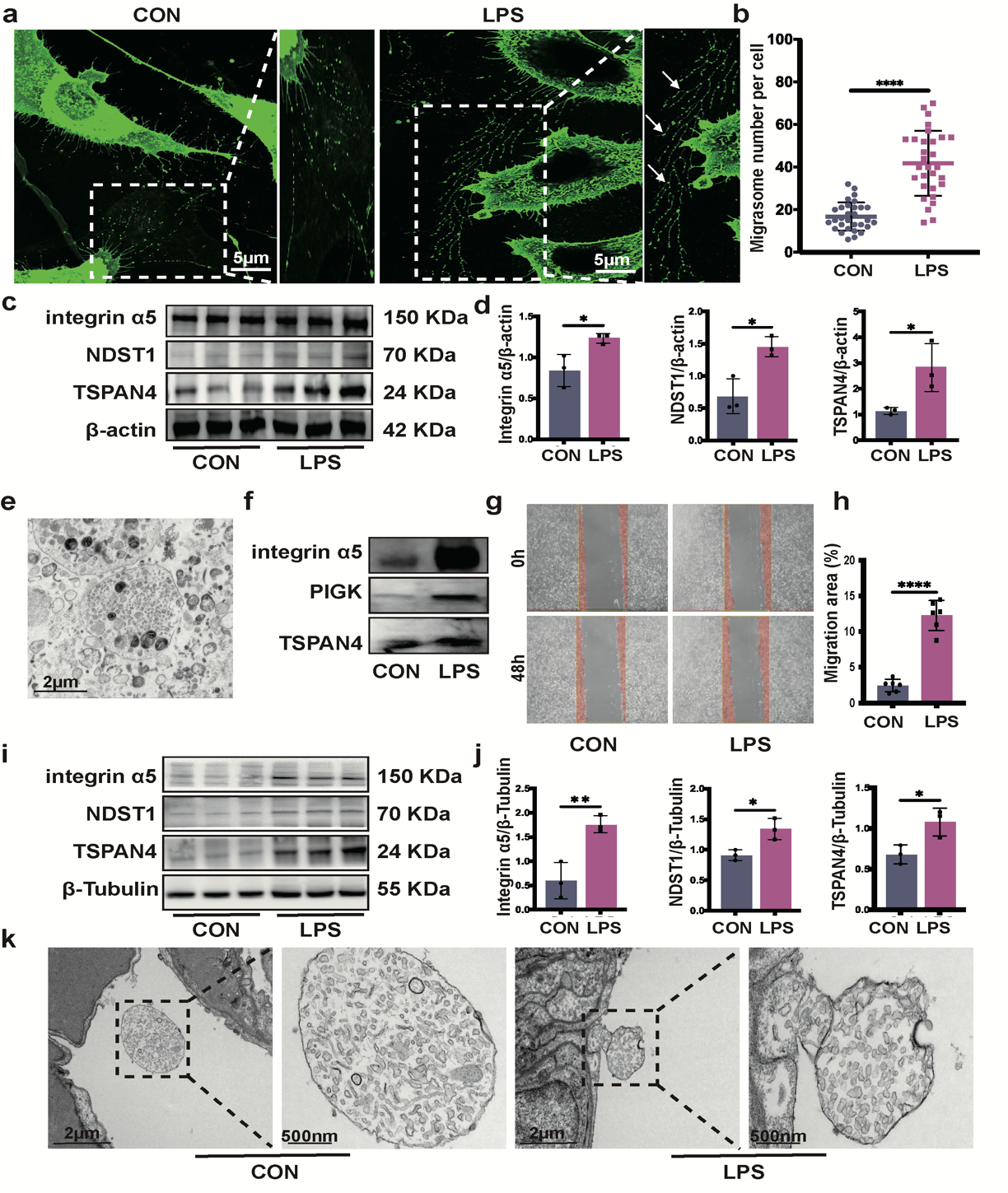
图1 LPS促进成纤维细胞源性迁移体释放
为进一步明确PGC-1α作为调控迁移体释放和mtDNA外漏的关键因子。通过构建过表达PGC-1α成纤维细胞稳转株进一步研究发现,过表达PGC-1α可显著改善线粒体稳态,减少胞质mtDNA积聚与迁移体释放,并降低迁移体被巨噬细胞摄取的水平,从而减少MMT细胞比例,缓解SAPF的发生发展。
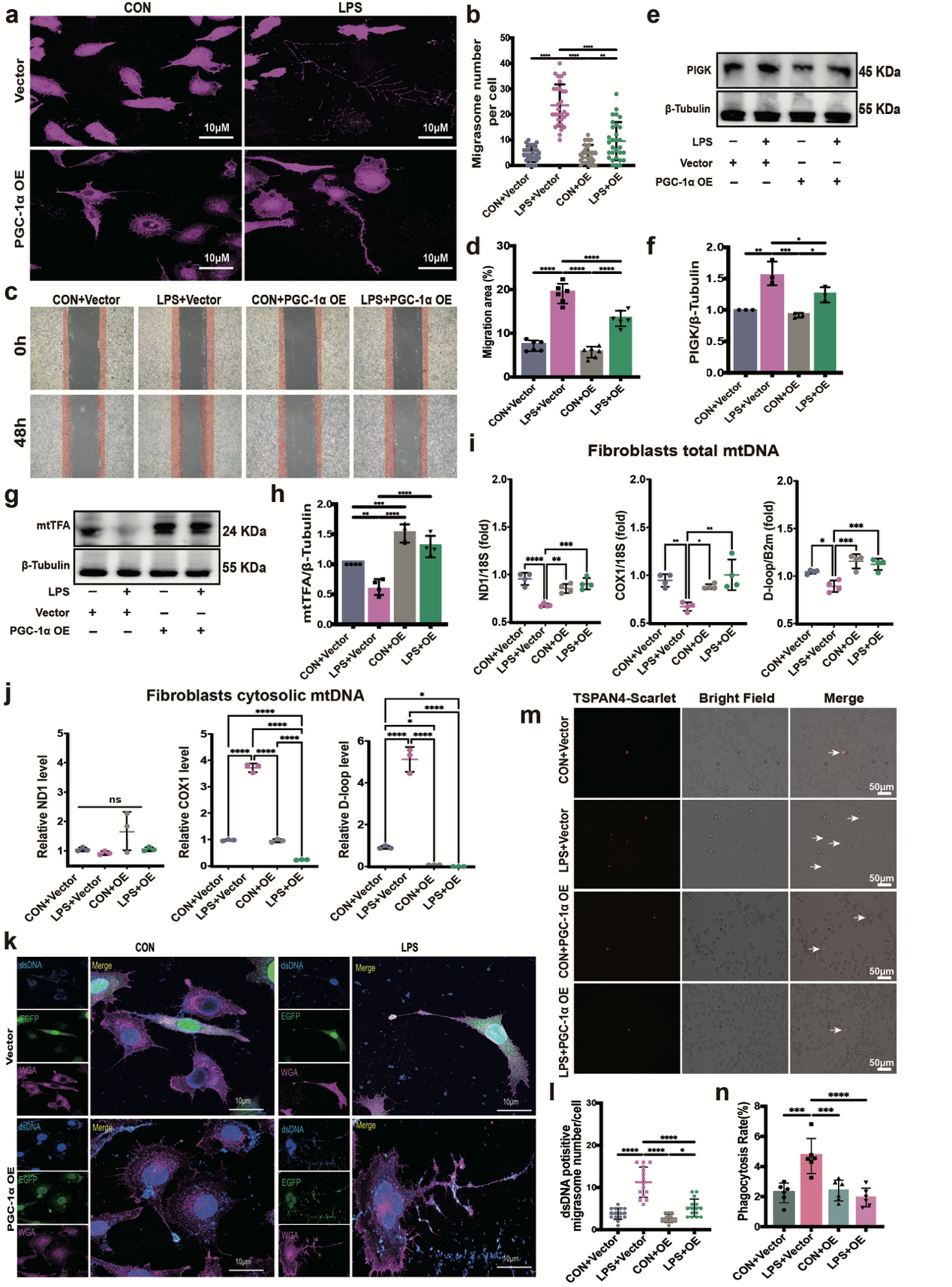
图2 过表达PGC-1α抑制LPS诱导的成纤维细胞源性迁移体释放
研究结论
综上所述,该研究揭示了PGC-1α调控迁移体释放并介导巨噬细胞–肌成纤维细胞转化(MMT)在脓毒症相关性肺纤维化(SAPF)中的关键机制。
研究发现,激活PGC-1α可改善线粒体稳态,抑制mtDNA迁移体释放,减少MMT发生,显著缓解SAPF病理进程。
该研究明确了迁移体在免疫细胞与间充质细胞间通讯中的作用,并提出PGC-1α作为SAPF干预的潜在靶点。
吉满助力
本研究中所构建的PGC-1α稳定过表达的成纤维细胞株及TSPAN4-mScarlet质粒均由吉满生物(Genomeditech)提供。
了解更多质粒构建,病毒包装,稳转株构建,敲除细胞株,报告基因检测等相关服务。欢迎访问吉满生物官网:www.genomeditech.com
免费咨询电话:400-627-9288