文献解读

2025年2月,美国德克萨斯州达拉斯德克萨斯大学研究人员在Nature Communications上发表题为“BBOX1 restrains TBK1-mTORC1 oncogenic signaling in clear cell renal cell carcinoma”的文章。
研究发现γ-丁酰基-β-羟基酶1(BBOX1)在透明细胞肾细胞癌(ccRCC)中常常表达缺失,数据表明恢复BBOX1的表达可以抑制ccRCC异种移植模型中的细胞活性和肿瘤形成。机制上BBOX1通过减弱DCLK2-TBK1致癌信号通路,在生理条件下拮抗mTORC1和糖酵解,从而发挥其抑制肿瘤生长的作用。
研究背景
在2022年,美国约有79,000例新发肾癌病例和13,390例死亡。透明细胞肾细胞癌(ccRCC)占肾癌的85%,是一种具有致命性的疾病,并且对化疗经典上具有抗药性。
ccRCC的主要致病机制涉及von Hippel–Lindau(VHL)基因失活,导致HIF2α的稳态维持,进而促进肿瘤生长。尽管一些HIF2α抑制剂显示出一定的治疗潜力,但仍然有相当一部分ccRCC对其耐药,强调了发掘新的治疗靶点的重要性。
项目研究
研究人员首先对TCGA数据库中与癌症患者结果相关的 BBOX1遗传特征进行分析发现,BBOX1基因表达与ccRCC患者的预后显著相关,高表达BBOX1的患者预后较好。
在ccRCC肿瘤组织中,BBOX1的mRNA和蛋白水平均显著低于正常肾组织,且这种下调与肿瘤的分期、分级和代谢特征相关。此外,BBOX1在ccRCC细胞系中也表现出特异性下调,尤其是在恶性转化的肾近曲小管细胞中。研究结果表明,BBOX1可能作为ccRCC的肿瘤抑制基因,其表达下调与ccRCC的发生和发展密切相关。
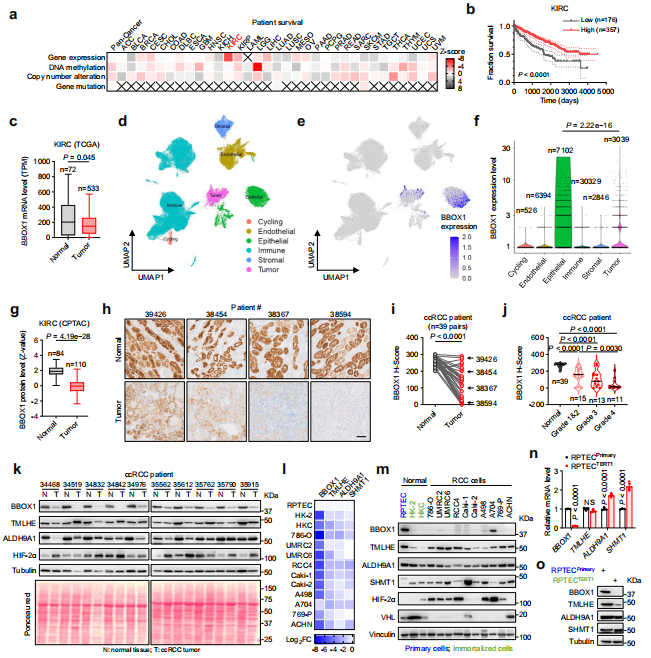
图1 BBOX1 在 ccRCC 中显著下调
为了研究 BBOX1 在 ccRCC 中的功能作用,通过体内外实验发现,BBOX1的高表达显著抑制了ccRCC细胞在体内形成的肿瘤生长,但在传统高营养培养基中对细胞增殖无明显影响。相反,在营养限制的生理条件下(如低葡萄糖和/或谷氨酰胺水平),BBOX1的恢复显著降低了细胞的存活率和锚定独立生长能力。
BBOX1 是一种具有已知晶体结构的代谢酶,因此研究人员构建了表达BBOX1的催化失活突变体(CD)的786-O细胞系进行体内异种移植实验,与野生型BBOX1相比,CD突变体无法抑制肿瘤生长,表明BBOX1通过酶活性在营养限制的生理条件下发挥肿瘤抑制作用。
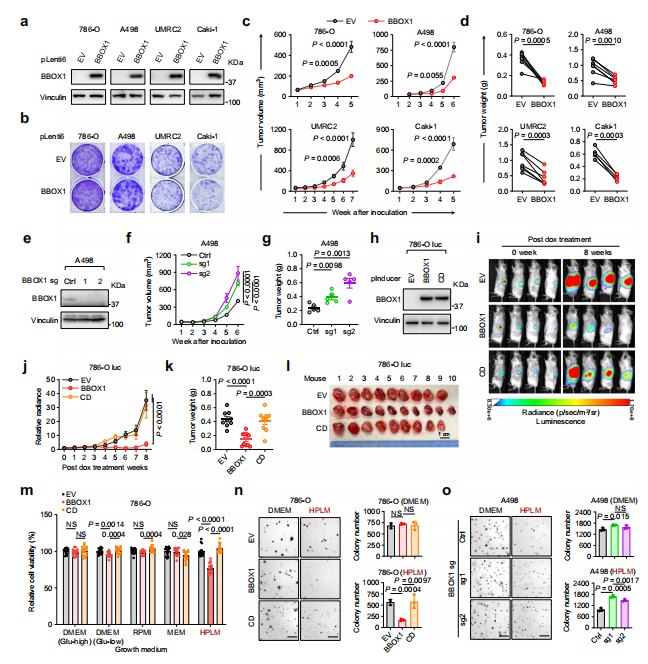
图2 BBOX1 重新表达抑制生理生长条件下 ccRCC 肿瘤发生和细胞生长
为了阐明 BBOX1 抑制 ccRCC 的分子机制,研究人员比较了BBOX1高表达的786-O细胞在体外(DMEM培养)和体内(异种移植肿瘤)的转录组数据,分析差异表达基因(DEGs)。研究发现,体内外差异表达基因之间几乎没有重叠,BBOX1在体内外的作用机制可能存在显著差异。
对体内肿瘤转录组进一步生信分析发现,BBOX1的恢复显著抑制了促进ccRCC肿瘤发展的mTORC1信号通路活性,而这种抑制作用在传统培养基中并未观察到,研究人员通过RT-qPCR、免疫荧光和免疫组化实验进一步验证了这一观点。
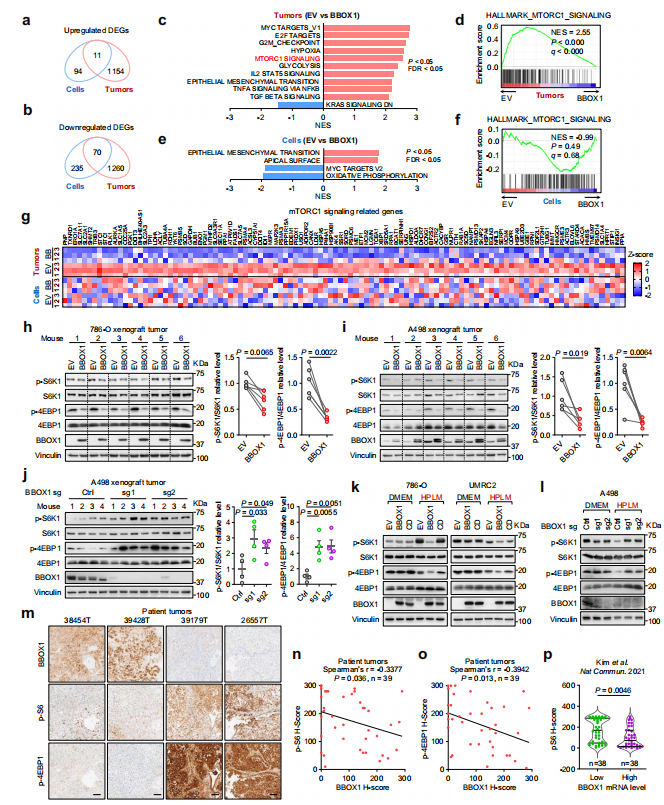
图3 BBOX1 减弱 ccRCC 中的 mTORC1 信号传导
ccRCC 的特征是糖酵解增强伴随着线粒体呼吸抑制,葡萄糖代谢对于这种类型的恶性肿瘤尤为重要。
因此研究人员通过体内外实验和代谢分析探讨BBOX1在透明细胞肾细胞癌(ccRCC)中对糖酵解途径的作用,结果发现,在营养限制的生理条件下,BBOX1恢复表达显著下调了肿瘤和786-O细胞中糖酵解相关基因的表达,并减少了糖酵解和三羧酸循环(TCA cycle)中间产物的积累,敲除细胞中BBOX1则促进了糖酵解的能力,但在传统高营养培养基中这种抑制作用不明显。
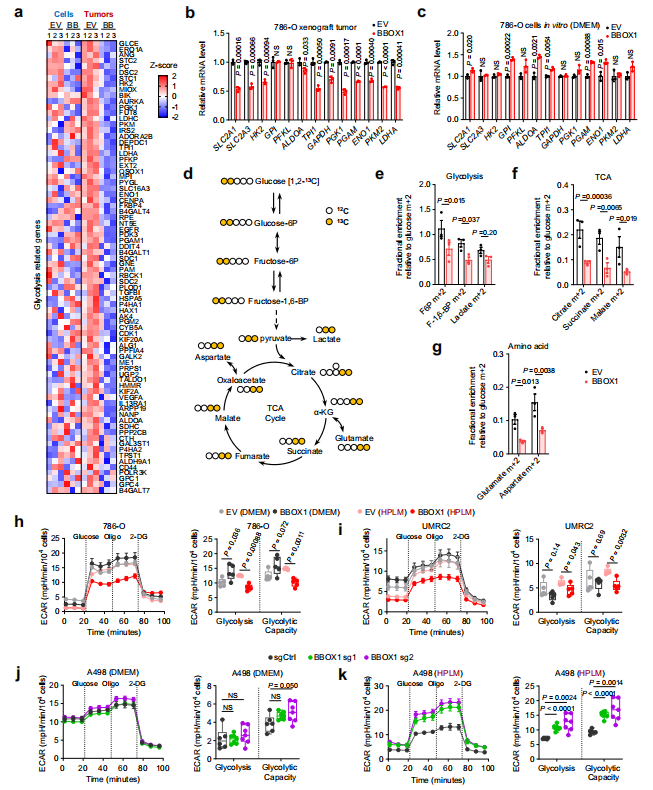
图4 BBOX1 在生理条件下抑制糖酵解
为了从机制上进一步了解 BBOX1 如何通过抑制 mTORC1 和糖酵解来控制 ccRCC 肿瘤发生,通过免疫沉淀-质谱分析(IP-MS)发现,TBK1是与BBOX1相互作用的顶级候选蛋白之一,在异种移植肿瘤中存在显著的内源性相互作用,且这种相互作用依赖于BBOX1的酶活性。
在细胞和皮下肿瘤实验中发现,TBK1的敲低显著抑制了由BBOX1敲除引起的mTORC1激活、糖酵解增加和细胞生长促进。TBK1是BBOX1介导的肿瘤抑制功能的核心介质,其活性对于BBOX1的功能至关重要。
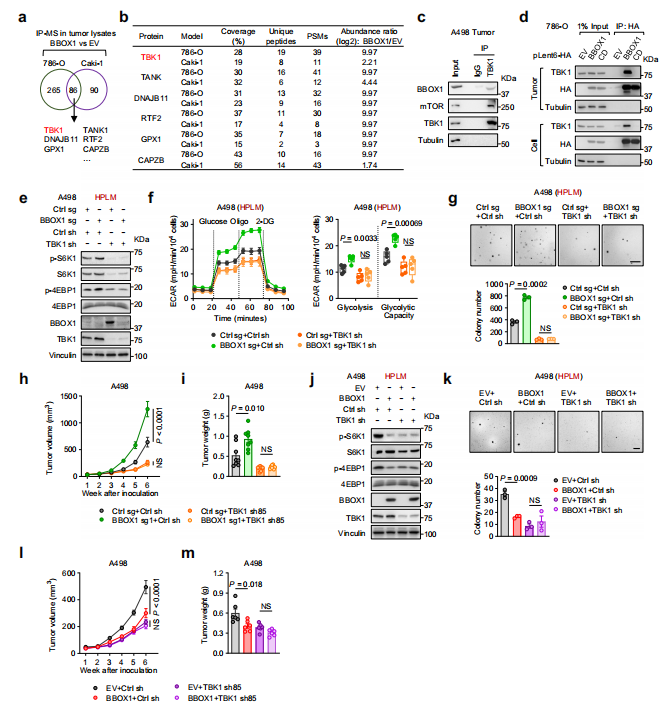
图5 确定 TBK1 是 ccRCC 中促进 BBOX1 发挥作用的关键介质
TBK1 已被证明在几种癌症模型中促进或抑制 mTORC1,然而,目前尚不清楚 TBK1 是否调节 ccRCC 中的 mTORC1 或其他促肿瘤途径(如糖酵解)。
通过体外细胞免疫印迹和ECAR实验表明,TBK1的敲低显著抑制了mTORC1信号通路的活性和糖酵解能力,而野生型TBK1或激活(S172D)突变体的过表达则显著促进了这些过程,但这种作用仅在营养限制培养基中观察到,在DMEM(高营养)培养基中未发现显著变化。
接下来进行小鼠体内异种移植肿瘤实验,结果显示肿瘤生长趋势和体外细胞实验结果一致,TBK1 仅在生理条件下促进 mTORC1和糖酵解。
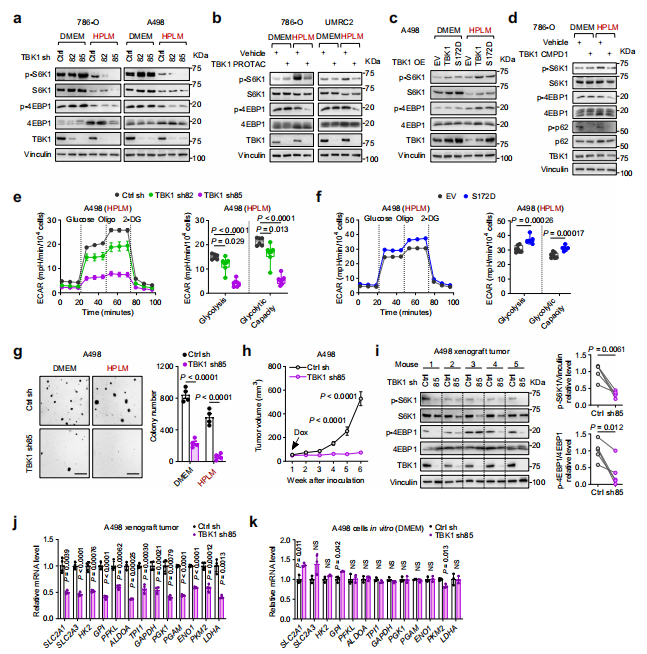
图6 生理条件下,TBK1 是 mTORC1 激活和糖酵解所必需的
接下来,研究者通过体内外实验和分子机制探讨BBOX1如何影响ccRCC中的TBK1信号转导。结果发现,BBOX1的表达与TBK1的活性呈负相关,免疫沉淀实验验证BBOX1与DCLK2可以直接相互作用,并通过阻断DCLK2-TBK1的结合来抑制TBK1的激活。这种抑制作用在营养限制的生理条件下尤为显著,并最终导致mTORC1信号通路和糖酵解途径的抑制。
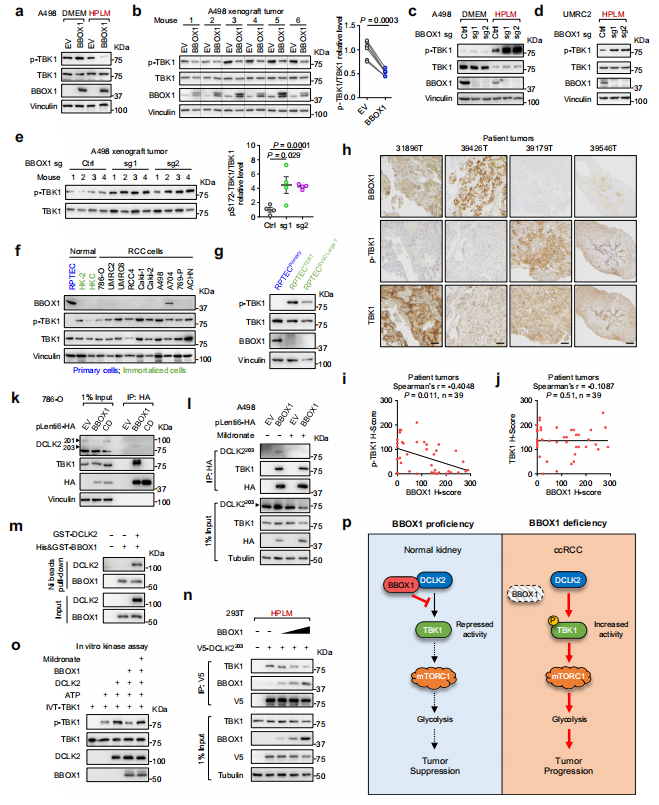
图7 BBOX1 负向调节 ccRCC 中的 TBK1 活化
吉满生物
如想了解更多质粒构建、病毒包装、稳转株构建、敲除细胞株、报告基因检测等相关服务。欢迎访问吉满生物官网:
免费咨询电话:400-627-9288